Nanochave de um único átomo controla todos os organismos vivos
Redação do Diário da Saúde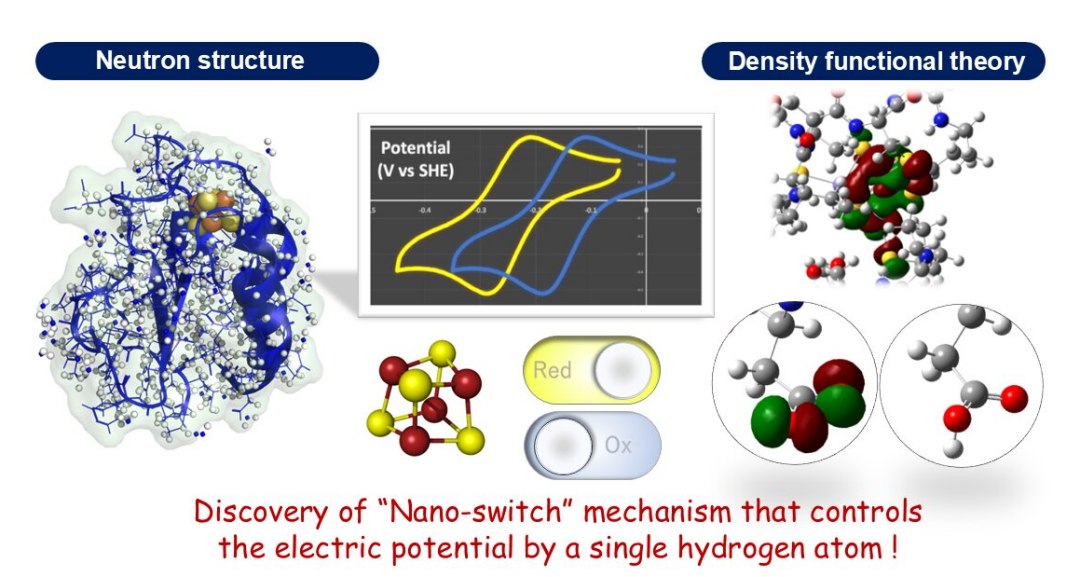
[Imagem: Kei Wada et al. - 10.7554/eLife.102506]
Nanochave da vida
Pesquisadores japoneses revelaram, pela primeira vez, que os seres vivos possuem uma chave minúscula, a menor possível, para controlar o processo que todos os organismos precisam ativar para obter energia e se manterem vivos.
É uma chave atômica, do tamanho de um único átomo de hidrogênio, responsável por acionar um mecanismo para controlar o potencial de uma proteína transportadora de elétrons na reação redox.
A maioria das reações nos organismos vivos envolve um processo de transferência de elétrons - é isto que é chamada de reação redox. Por exemplo, a respiração e a fotossíntese podem ser classificadas como reações redox.
Algumas proteínas que auxiliam na transferência de elétrons contêm ferro e enxofre. A descoberta fundamental é que o potencial elétrico do aglomerado ferro-enxofre muda drasticamente dependendo da presença ou ausência de um único átomo de hidrogênio na cadeia lateral de um aminoácido, um mecanismo que a equipe chamou de nanochave, ou nanointerruptor.
A ferredoxina é uma pequena proteína que contém aglomerados de ferro-enxofre e é conhecida como transportadora de elétrons nos organismos vivos. É uma proteína universal, que se acredita estar presente em quase todos os organismos vivos; no entanto, o mecanismo pelo qual a ferredoxina transporta elétrons de forma estável permanecia um mistério até agora.
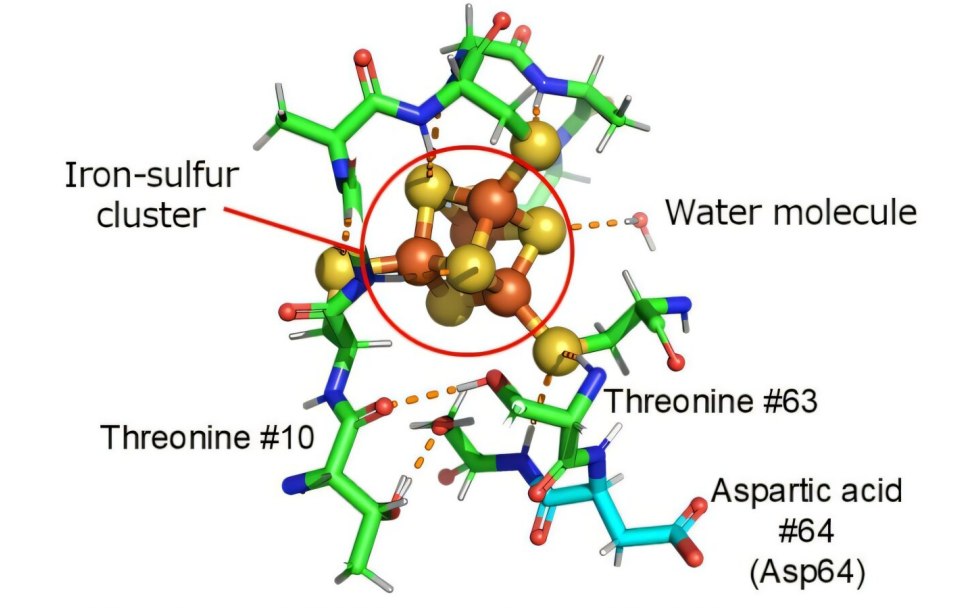
[Imagem: Kei Wada et al. - 10.7554/eLife.102506]
Mecanismo universal
Os pesquisadores descobriram que um resíduo de aminoácido (ácido aspártico 64), localizado longe do aglomerado ferro-enxofre, tem um efeito significativo na probabilidade da transferência de elétrons no aglomerado, e desempenha um papel como um interruptor - a nanochave - que controla a transferência de elétrons na ferredoxina.
Além disso, o estudo descobriu que o mecanismo é universal em organismos.
Além de elucidar em elemento fundamental da biologia dos seres vivos, os cientistas afirmam que a descoberta deverá ter uso imediato no desenvolvimento de sensores ultrassensíveis para oxigênio e óxido nítrico e para novos medicamentos.
Artigo: Protonation/deprotonation-driven switch for the redox stability of low-potential [4Fe-4S] ferredoxin
Autores: Kei Wada, Kenji Kobayashi, Iori Era, Yusuke Isobe, Taigo Kamimura, Masaki Marukawa, Takayuki Nagae, Kazuki Honjo, Noriko Kaseda, Yumiko Motoyama, Kengo Inoue, Masakazu Sugishima, Katsuhiro Kusaka, Naomine Yano, Keiichi Fukuyama, Masaki Mishima, Yasutaka Kitagawa, Masaki Unno
Publicação: eLife
DOI: 10.7554/eLife.102506
| Ver mais notícias sobre os temas: | |||
Biologia | Alimentação e Nutrição | Vitaminas | |
| Ver todos os temas >> | |||
Descoberta uma forma inteiramente nova de vida dentro dos seres humanos
Emoções positivas e sono profundo melhoram a retenção da memória
Mangas melhoram a sensibilidade à insulina e o controle da glicose no sangue
Ciência desbanca conceito de meritocracia
IA descobre conexões ocultas entre doenças
Fundações da inteligência humana são observadas pela primeira vez
Evolução não é cega e nem aleatória: Há uma "previsão" na evolução
Cientistas identificam 15 motivações básicas do comportamento humano
Especialistas desaconselham fortemente injeções na coluna contra dor crônica nas costas
Bactérias invadem cérebro após implante de chips neurais
Banho de chuveiro com bolhas ultrafinas cura problemas de pele
Revolução na dermatologia e cosmética: Ciência estava errada sobre colágeno da nossa pele
Bactérias invadem cérebro após implante de chips neurais
Amantes se encaixam em quatro categorias
Você (também) fica entediado nas suas práticas espirituais?
Estudo inédito sobre memória mostra que nem tudo funciona como imaginávamos
Ponto de transição sinaliza o início do fim do relacionamento
Cientistas identificam 15 motivações básicas do comportamento humano
Mangas melhoram a sensibilidade à insulina e o controle da glicose no sangue
IA descobre conexões ocultas entre doenças
Vacina do Butantan contra dengue grave tem 89% de proteção
Brasil tem primeiras mortes por febre oropouche no mundo
Censo 2022: Por que várias cidades brasileiras tiveram diminuição da população?
Brasil tem primeiro caso de gripe aviária em aves domésticas
Brasil decreta emergência zoossanitária devido à gripe aviária
Proibido o uso de animais em pesquisas de cosméticos e higiene pessoal
A informação disponível neste site é estritamente jornalística, não substituindo o parecer médico profissional. Sempre consulte o seu médico sobre qualquer assunto relativo à sua saúde e aos seus tratamentos e medicamentos.
Copyright 2006-2025 www.diariodasaude.com.br. Todos os direitos reservados para os respectivos detentores das marcas. Reprodução proibida.


